|
「今まで使っているガソリンや軽油などの燃料に混ぜても、設備や部品を特別に改造することなく使える燃料」のことを言います。
自動車や飛行機、発電所など、世の中には様々な「燃料を燃やしてエネルギーを得る」という「内燃機関」がありますが、使う燃料の種類によって、構造はそれぞれ異なります。例えば自動車は「ガソリン車」は「ガソリン」、「ディーゼル車」は「軽油」を燃料として使いますが、それぞれ燃料の燃える性格を生かした構造となっており、特に点火の方法が異なります。
では、「軽油の方が安いから、ガソリン車に入れちゃえ!」「軽自動車には軽油のはず」と給油してしまったらどうなるでしょうか? この場合まったくエンジンがかからないどころか、エンジン本体が壊れる可能性があります。逆の「ディーゼル車にガソリン」の場合、更に深刻な状態になります。ガソリンスタンドで同じように販売されていても、「ガソリン」「軽油」は「蒸発しやすさ」「燃えやすさ」などが大きく離れた別の液体です。通常はエンジンや設備の燃焼方法に合っていない、設計・開発者の想定と異なる燃料を入れてはいけないのです。
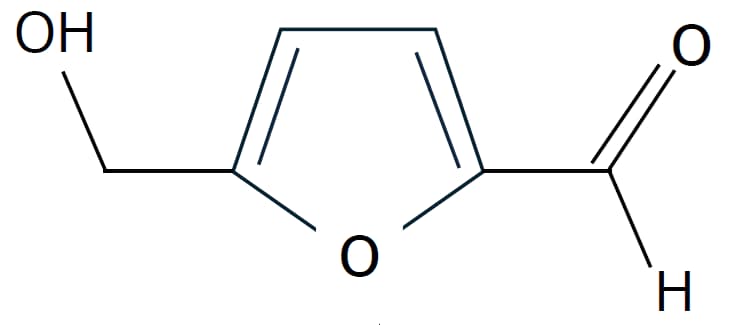
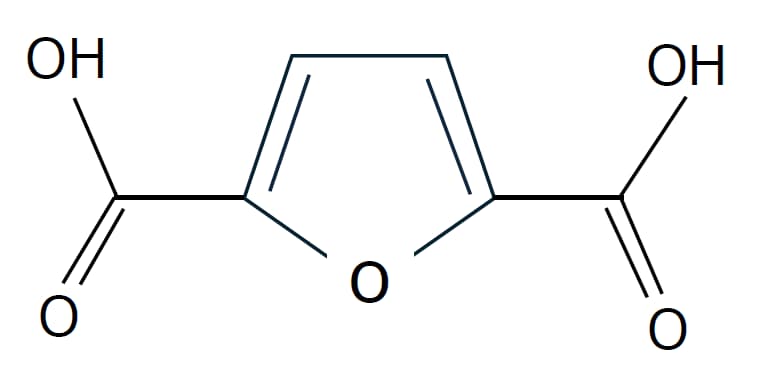
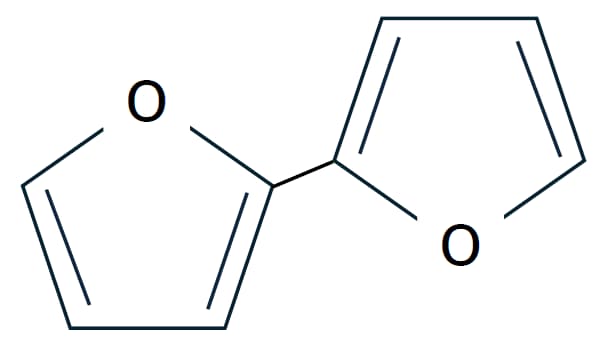
しかし近年、持続可能な社会を考える上で「従来の燃料に混ぜても、内燃機関や設備を交換せずそのまま使える」というドロップイン燃料が注目されています。なるべく元の燃料の性格に近い物質を代わりに、或いは混合して使うというもので、ガソリンへのエタノール混合や、飛行機用燃料への実用化が既にされています。E-fuelの合成ガソリンや、Bio-fuelのBio-Diesel・バイオエタノールなどを用いることで、カーボンニュートラルによる温暖化防止にもつながる取り組みです。
ただし、性格は似ているとはいえ、完全に同じ物質でないことが開発の壁にもなります。その一つの例えで「ガソリンとエタノールの蒸発特性の違い」を挙げてみます。
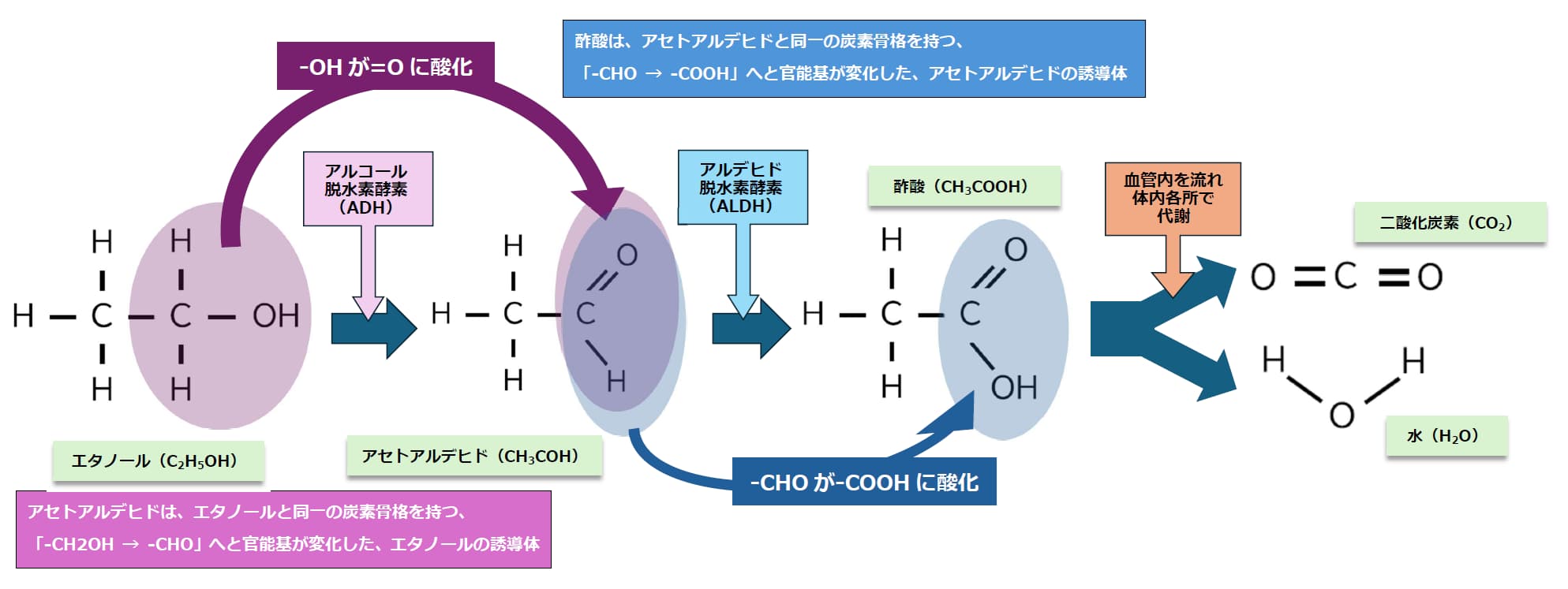
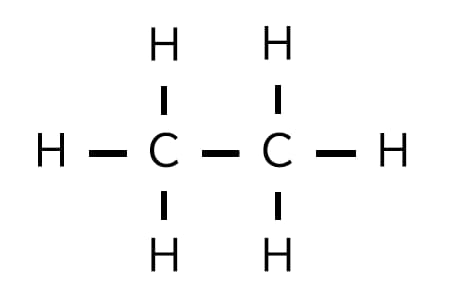
最近「エタノール(C2H5OH)混合ガソリン」が一般的に使われるようになってきています。C2H5OHはガソリンに分離せずに混ざりやすく、運転を安定させるメリットがあり、またバイオマス由来のものにすれば、カーボンニュートラルに近づくことになります。
C2H5OHは消毒でお馴染みですが、皮膚につけると直ぐに蒸発してヒンヤリします。これはC2H5OHの「周りの熱を奪って蒸発しやすい」という性格(専門用語でいうと「気化熱が大きい」)によるものです。物理的な値からも、熱の奪いやすさは「エタノール > ガソリン」というデータがあります。
一方ガソリンは、セルフスタンドで車の給油をしたことがある人はわかりますが、給油口の蓋を外すと気体になったガソリンが「シューッ」と音がして抜けるのがわかると思います。蒸発しやすいとはいえ、通常の生活でC2H5OHの瓶を開けただけでは蒸発した気体が音を立てて漏れることはありませんので、感覚的にも常温での蒸発しやすさ(専門用語でいうと「揮発性の高さ」)は「ガソリン > エタノール」ということがわかります。
ガソリン車のエンジンは、そのガソリンの「蒸発のしやすさ」を活かした作りになっています。ここで「蒸発しやすさはガソリンより弱く、また周りの熱はガソリンより奪いやすい」というエタノールを多く入れすぎるとエンジン内を冷やし、更に最初に点火するとき(冷始動時)の性能が落ちる可能性が高まります。
他に課題もありますが、逆に言うと、このような問題点を解決することがドロップイン燃料の可能性を広げます。安全に効率よく使える物質の選定や混合割合などの研究が、燃料と内燃機関両方で進んでいます。
|



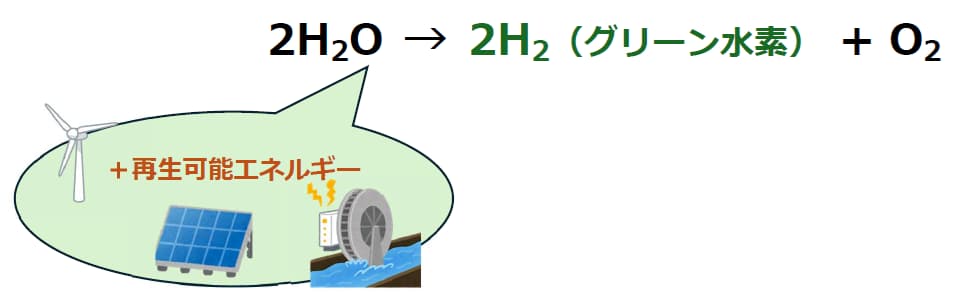

 2H2O → 2H2 + O2
2H2O → 2H2 + O2